发布日期:2025-04-15 来源:中科蓝海(天津)科技有限公司
紫外可见分光光度计作为一类至关重要的分析仪器,基于紫外可见分光光度法原理,利用物质分子对紫外可见光谱区的辐射吸收来进行定性定量分析,其应用范围极为广泛,横跨了物理学、化学、生物学、医学、材料科学、环境科学等众多科学研究领域,它扮演着不可或缺的角色,助力科学家们深入揭示自然界的奥秘。

一、基础原理与结构
物质的吸收光谱本质上就是物质中的分子和原子吸收了入射光中的某些特定波长的光能量,相应地发生了分子振动能级跃迁和电子能级跃迁的结果。由于各种物质具有各自不同的分子、原子和不同的分子空间结构,其吸收光能量的情况也就不会相同。因此,每种物质就有其特有的、固定的吸收光谱曲线,可根据吸收光谱上的某些特征波长处的吸光度的高低判别或测定该物质的含量,这就是分光光度定性和定量分析的基础。
紫外可见分光光度法定量分析的基础是朗伯-比尔(Lambert-Beer)定律。即物质在一定浓度的吸光度与它的吸收介质的厚度呈正比,其数学式如下:
A=abc
A——吸光度;
a——摩尔吸光系数;
b——吸收介质的厚度;
c——浓度。
不同的物质有各自喜爱的特定波长的光,我们通过机器检测出物质的特定吸收波长,就可以对样本进行定性分析。另外,物质浓度越高,对特定的波长吸收度也会增高且成正比例关系,我们通过光度计测得吸光度值再通过朗伯比尔定律公式就能得出样本浓度。
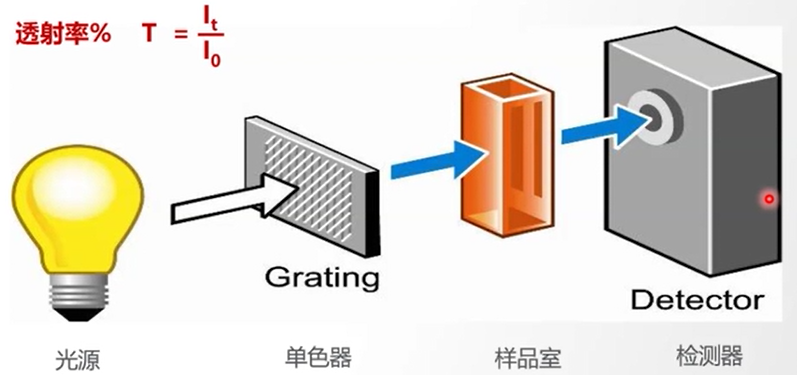
一般地,紫外可见分光光度计主要由光源、单色器、样品室、及检测系统组成。光源发出的复合光通过单色器被分解成单色光,当单色光通过样品室时,一部分被样品吸收,其余未被吸收的光到达检测器,被转变为电信号,经电子电路的放大和数据处理后,通过显示系统给出测量结果。
二、功能及参数
1. 吸光度检测
测量样品某一个波长处的吸光度,所有型号的产品都具有光度测量的功能,光度计测量的样品一般都是液体,有极个别的用户测量的是固体,这种情况一般测量的是透过率 T 值(透光率),比如玻璃或材料科学研究等。
2. 浓度直读
在光度计上建立工作曲线法-建立浓度与 T/A 的坐标关系,机器通过测量样品吸光度后会自动套用公式换算出具体浓度,直接显示浓度数值。
3. 光谱扫描(定性分析)
测量物质的最大吸收波长在多少 nm 处,自然界的物质一般都有自己特定的吸收谱图,就像人的指纹一样,所以得到样本的吸收谱图就可以判断未知样本是什么。
4. 时间扫描(动力学检测)
在浓度检测的基础上设置自动检测间隔时间,用来观察样品浓度随时间变化的曲线,比如:酶制剂行业,用来测量酶制剂在几分钟内的吸光度的变化值,一般每隔 30 秒测量一个数据。
5. 多波长测定
一次性测定物质在多个波长下的吸光度。比如:叶绿素的国标测定方法,需要测定 750/663/645/630nm 共 4 个波长处的吸光度,总氮检测需要在两个波长下进行检测, 220nm/275nm。
三、分析及应用
1. 定性分析
把试样的光谱特征,如吸收峰的数目、位置、强度(摩尔吸收系数)以及吸收峰的形状(极大、极小和拐点),与纯化合物或者文献报道的标准紫外光谱图做比较,推测化合物的结构,检查化合物的纯度。
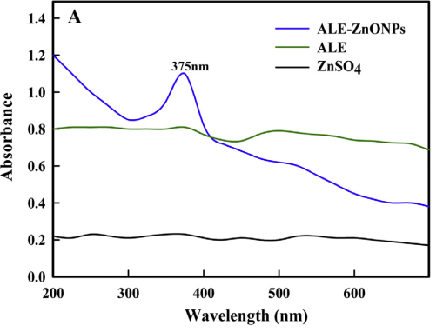
ALE-ZnONPs、ALE 和 ZnSO4 的紫外-可见吸收光谱图
沙特阿拉伯国王大学 Mansour S. Al-Said 等人利用紫外-可见吸收光谱确定所制备的样品 ALE-ZnONPs 中含有氧化锌纳米颗粒。如上图所示,样品 ALE-ZnONPs 在 375nm 出现了特征峰,制备样品的原材料 ALE 和 ZnSO4 在该处无特征峰。根据文献报道,纳米氧化锌的特征峰在 358-375nm 之间,由此证实了氧化锌纳米颗粒的生成。
根据吸收峰的强弱对比比较样品的相关性质。一种化合物可能拥有多个吸收峰,这些峰的相对强弱变化可以推测出化合物的相关性质。首先是根据文献了解化合物的每个吸收峰所代表的含义,再进行对比。
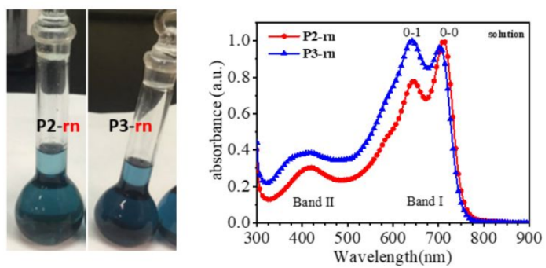
P2-rn、P3-rn溶解性光学照片和紫外-可见吸收光谱图
以基于异靛蓝的聚合物 P2-rn 和 P3-rn 为例进行说明。在这类基于异靛蓝的 D-A 聚合物中,一般具有两个吸收带,band I 和 band II。band I 又细分为 0-0 峰和 0-1 峰等,其中 0-0 峰表示分子的聚集状态,越高说明聚集越强。这两个聚合物结构的差异仅在其中一条烷基侧链的大小不同,P3-rn 的烷基侧链比 P3-rn 的多出 8 个 C 原子。
从图中紫外-可见吸收光谱图可以看出,从 P2-rn 到 P3-rn,0-0 峰的强度/0-1 峰的强度减小,说明 P3-rn 在溶液中的聚集更弱,这和溶解性对比图所示相吻合,相同浓度下,P3-rn 的溶解性明显较好,即分子更不易聚集,分散的更好。
2. 半定量分析
根据吸收峰的强弱对比比较样品的浓度大小关系。四川大学的郭熠等人利用紫外-可见吸收光谱对比了溶液中多硫化锂的含量,从而进一步对比了样品 GSVm 和 GSm 对多硫化锂的吸附能力的强弱。将样品 GSVm 和 GSm 分别放入相同浓度的多硫化锂溶液中,静置一段时间。样品吸附多硫化锂后,溶液中的多硫化锂浓度改变。
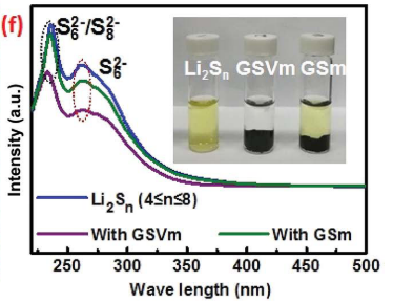
浸泡了 GSVm 和 GSm 的 Li2Sn 溶液的光学照片和吸附后对应溶液的紫外-可见吸收光谱图
如图所示,测定吸附后溶液的紫外-可见吸收光谱,对比吸收峰的强弱,可以看出相较于原始的多硫化锂溶液,加入样品 GSVm 和 GSm 吸附后的多硫化锂溶液吸收峰强度均降低,并且加入样品 GSVm 吸附后的多硫化锂溶液吸收峰强度下降更多,说明样品 GSVm 吸附多硫化锂能力更强,使溶液中多硫化锂浓度下降更多。
3. 定量分析
单组分定量分析:
(1)标准曲线法:直接分取标准溶液进行光度测定或显色测定所测得的吸光度与浓度作图得到的曲线。
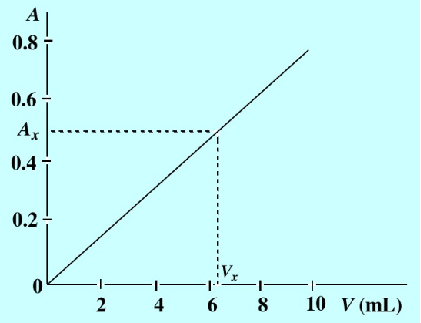
标准曲线法校正曲线
(2)标准加入法(增量法):把未知试样溶液分成体积相同的若干份,除其中的一份不加入被测组分标准试样外,在其他几份中都分别加入不同量的标准试样,然后测定各份试液的吸光度,并绘制吸光度对增量的校正曲线。
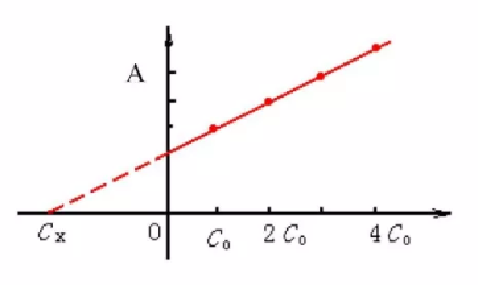
增量法校正曲线
多组分定量分析:在多组分体系中,如果各组分对光都有吸收并且无相互作用,这时体系的总吸光度则等于各个组分的吸光度加和,这就是光吸收的加和特性。解决多组分混合物中各个组分测定的基础是吸光度的加和性。对于一个含有多种吸光组分的溶液,在某一测定波长下,其总吸光度应为各个组分的吸光度之和。
示差分光光度法:普通分光光度测定在很低或者很高吸光度范围内进行定量分析时相对误差较大,因此不适于高含量或痕量物质的分析,可以采用示差分光光度法进行测定。示差分光光度是用一个已知浓度的标准溶液作为参比,与未知浓度的试样溶液比较,测量其吸光度。
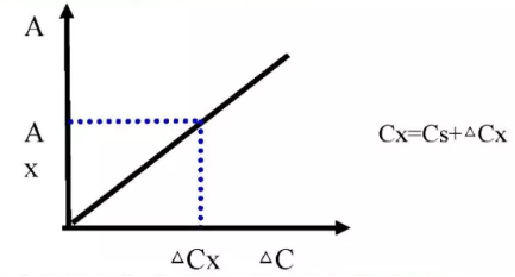
示差法校正曲线
昆明医科大学的邓菊庆等人采用紫外分光光度法测定了 5 种柑橘皮中总黄酮的含量。将样品溶液、芦丁标准液、空白对照液显色后在 200-800nm 波长进行扫描,选定最大吸收峰 510nm 作为测定波长。于 510nm 波长下测定不同浓度芦丁标准液的吸光度,以芦丁标准品浓度为横坐标、吸光度为纵坐标绘制标准曲线,进行线性回归。从线性相关方程计算出相应的黄酮浓度 C,再换算成提取液中总黄酮的质量,从而计算出总黄酮含量。
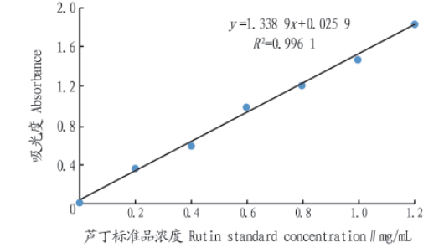
芦丁标准曲线
4. 原位紫外-可见吸收光谱法
通过原位紫外-可见吸收光谱图中吸收峰位置或者强度的变化可以分析样品在反应过程中的成分变化或者浓度变化。
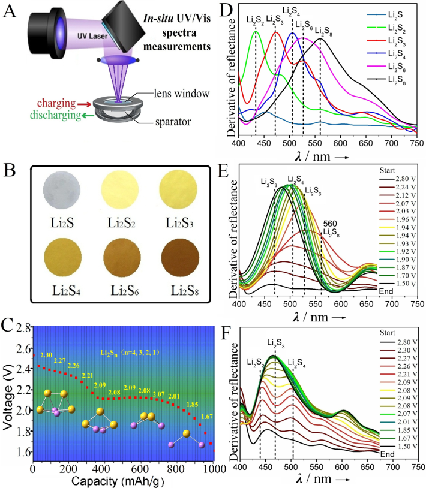
(A)原位紫外-可见吸收光谱法测试电池装置示意图;(B)不同硫化物在电解液中的光学照片;(C)锂硫电池放电时电压-容量曲线图;(D)不同硫化物在电解液中的紫外-可见吸收光谱图;电极 S-rGO(E)和电极 S-GSH(F)在放电过程中的紫外-吸收光谱图
为了探究锂硫电池在放电过程中巯基与硫共聚物的反应机理,苏州大学的 Na Xu 等人利用原位紫外-可见吸收光谱法测试了锂硫电池在第一次放电时硫化物成分的变化情况。图 A 为测试装置示意图。首先制备了 Li2S、Li2S2、Li2S3、Li2S4、Li2S6、Li2S8 溶液(溶剂为电解液),通过紫外-吸收光谱法得到了对应的吸收峰(图 D)作为参考。测定电池在放电过程中的紫外-可见吸收光谱,通过比对吸收峰的位置,确定了电极 S-GSH(图 F)在放电过程中并未有长链多硫化锂(Li2S6、Li2S8)的产生。
5. 误差分析:对朗伯-比耳定律的偏离
标准曲线法测定未知溶液的浓度时,发现标准曲线经常发生弯曲,这种现象称为对朗伯-比耳定律的偏离,如下图所示。
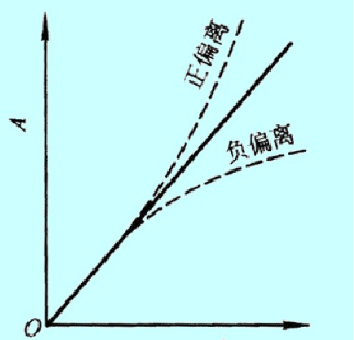
光度分析的工作曲线
主要原因是目前仪器不能提供真正的单色光,实际上仪器所提供的入射光是由波长范围较窄的光带组成的复合光。由于物质对不同波长光的吸收程度不同,因此引起了偏离。
为克服非单色光引起的偏离,首先应选择较好的单色器,此外还应将入射波长选定在待测物质的最大吸收波长且吸收曲线较平坦处。另外,当溶液浓度较大时,吸光质点可能发生缔合等相互作用,影响对光的吸收。因此,朗伯-比耳定律只适用于稀溶液。